界面活性剤とは、「界面に作用して界面の性質を変化させる物質」のことを言います。
ただ、一般的には水に混ぜて使用されるので、水と油のように混ざりにくい物質を分離させずに混ざるようにする物質と説明されることが多いです。
界面活性剤が2つの物質を混ざるようにする理由は、その構造にあります。
界面活性剤は下記のように、親水基と疎水基が両側に位置するような分子構造となってます。これにより2つの物質の間を仲介するような役割を果たしてくれるため、物質間で表面張力が抑えられ混ざりやすくなります。

界面活性剤は界面に集まるため、水に界面活性剤を溶かすと、油だけでなく空気との界面においても界面活性剤は集まります。
表面張力の低下
2つの物質が混ざる理由は、界面活性剤により表面張力が低下することが大きく影響しています。
表面張力が小さくなると、接する表面が大きくなりやすいので、つまり濡れが大きくなります。この特徴が洗浄に有利に働くため、界面活性剤は油汚れを落とす際に用いられます。
水の表面張力は他の液体に比べて非常に大きいため、水で洗浄する上では界面活性剤の役割は非常に重要といえます。
界面活性剤を入れると乳化しやすくなるという特性もありますが、これも表面張力低下により分離が抑えられるためです。そのため、界面活性剤が入った物質は一度混ぜると分離するまでに非常に時間がかかります。
ミセル構造
界面活性剤を入れると界面に集まりますが、どんどん濃度を増やしていくとミセル構造ができます。
ミセル構造とは、界面活性剤同士が集まって塊になったもののことを言います。
界面活性剤は疎水基をお互いに向けることでミセル構造を作り、表面が親水基で覆われた塊を作るようになります。
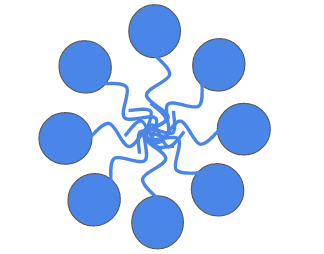
界面活性剤の濃度が少ないと球状のミセル形状となりますが、濃度が上がるにつれて棒状ミセルや層状ミセルに変化していきます。
ここでは水を対象としたため、上記のように外側を親水基とするミセル構造になりました。一方で、炭化水素のような有機溶媒の場合は疎水基を外側とする逆ミセル構造を取ります。
可溶化力
上記のミセル構造では、疎水基を中心として界面活性剤が集まっていました。
この中心部分は疎水基であるため、水に溶けない物質を包んでやることができます。ここに油汚れを集めて洗い流すのが、洗剤です。
可溶化力とは、このミセル内部に油汚れなどの油性物質を取り込む力のことです。
分類
界面活性剤は大きく分類して4つに分けられます。
アニオン界面活性剤
水に溶けた際に、親水基が陰イオンに電離する界面活性剤をアニオン界面活性剤といいます。
せっけんや合成洗剤に利用されています。
カチオン界面活性剤
水に溶けた際に、親水基が陽イオンに電離する界面活性剤をアニオン界面活性剤といいます。
逆性石けんとも呼ばれます。
マイナスに帯電している物体に吸着しやすく、殺菌性などがあるため、殺菌剤、防カビ剤、防錆剤、化粧品などに利用されます。
非イオン界面活性剤
非イオン系界面活性剤は、天然油脂類から得られた脂肪酸を水素還元して得られる高級アルコールが原料となっています。
沸騰水にも溶けるような強力な親水性をもたせたり、乳化及び洗浄力に優れたものも作成できる。
両性界面活性剤
イオン性が少なく、生体への影響が小さいので、体を洗うために利用されます。そのため、リンスやシャンプー、柔軟剤といったものに利用されています。
おわりに
今回は界面活性剤について簡単に説明しました。
親水基と疎水基の構造により表面張力を小さくすることで、様々な複雑な現象が現れます。ぜひ基本的な仕組みだけでも理解しておくと物質の特徴を理解しやすくなるでしょう。
 ITとCFD入門サイト
ITとCFD入門サイト